|
全球传染性病毒的持续暴发正深刻重塑人类健康安全格局。近年来,以SARS-CoV-2为代表的冠状病毒疫情,不仅对公共卫生体系构成严峻考验,也倒逼抗病毒药物研发向机制创新与策略升级加速演进。中国科学院昆明植物研究所植物化学与天然药物全国重点实验室郝小江团队长期聚焦天然产物抗病毒化学生物学研究,系统构建了从广谱活性发现到分子机制解析的完整研究体系。早期研究发现,菲啶类生物碱如(+)-lycoricidine对丙型肝炎病毒(HCV)具有显著抑制活性,其机制在于下调宿主热休克蛋白Hsc70而非直接作用病毒本身。基于此,团队开展系统构效关系(SAR)研究并持续优化结构,在显著降低细胞毒性的同时保持乃至提升抗HCV活性,为宿主靶向抗病毒(HTA)策略奠定了坚实的化学基础(Bioorg Med Chem Lett, 2013, Future Med Chem, 2015,)。进一步拓展至冠状病毒领域后,团队筛选获得多种高效抗猪流行性腹泻病毒(PEDV)化合物,并阐明其通过降低Hsc70 mRNA稳定性抑制蛋白表达,从而阻断病毒复制。在仔猪体内实验中,该类化合物展现出显著抑制病毒复制的效果,成为最早一批具备宿主靶向机制的潜在抗PEDV候选药物。这一系列工作不仅拓宽了菲啶类化合物的抗病毒谱系,也从机制层面验证了宿主蛋白调控作为广谱抗病毒策略的可行性(J Nat Prod, 2021)。
新冠疫情暴发后,团队迅速实现研究范式跃迁,聚焦SARS-CoV-2构建“双轨并行”研究路径:一方面,突破传统对酶类靶点的依赖,提出“结构蛋白亦可成药”的设想,围绕长期被忽视的核衣壳蛋白(N蛋白)开展系统探索。基于晶体结构开展理性设计,获得一系列高亲和菲啶类衍生物,首次发现了通过靶向N蛋白NTD区显著抑制病毒复制的活性化合物(Euro J Med Chem, 2022)。在此基础上,引入深度学习模型(EMPIRE、DeepFrag),实现从理性设计向AI驱动优化的跨越,构建并高通量筛选4万余个分子,成功获得候选活性化合物,其对N蛋白表现出纳摩尔级结合能力,并通过干扰N蛋白-RNA相互作用发挥抗病毒效应。该研究实现了结构生物学与人工智能的深度融合,既验证了N蛋白作为新型抗病毒靶点的可成药性,也展示了智能化手段在先导化合物快速发现中的变革潜力(Eur J Med Chem, 2024)。
另一方面,团队聚焦病毒复制核心酶非结构蛋白12(NSP12,RNA依赖性RNA聚合酶,RdRp),首次揭示其通过劫持宿主分子伴侣Hsc70逃逸伴侣介导自噬(CMA)降解、从而促进自身稳定与病毒复制的关键机制。研究发现,Hsc70在NSP12命运调控中具有动态双重功能,而病毒通过增强NSP12与Hsc70的结合、削弱其与LAMP2a的相互作用,重塑这一平衡以利于自身复制。基于该机制,团队开发出菲啶类小分子Hlyc41,能够竞争性结合Hsc70 F428位点,恢复Hsc70-LAMP2a互作,促进NSP12的CMA依赖性降解,从而有效抑制病毒复制。该研究揭示了SARS-CoV-2复制调控的新机制,为宿主靶向抗病毒策略提供理论依据,而菲啶小分子Hlyc41不仅为SARS-CoV-2 NSP12调控机制提供了新见解,也为基于病毒—宿主蛋白互作的小分子抗病毒药物设计开辟了新方向。
上述研究成果以Insights into SARS-CoV-2 replication control via targeting the host hijacking function of NSP12为题,近日在线发表在国际期刊Acta Pharmaceutica Sinica B上,中国科学院昆明植物所郝小江、陈铎之研究员为通讯作者,樊世瑞博士后为第一作者,本研究承蒙南京农业大学姚火春/刘广锦团队,中国科学院昆明动物研究所郑永唐团队,中国医学科学院医学生物学研究所(昆明)等单位的大力协助,研究获得中国科学院B类先导专项、中国医学科学院院医学科学创新基金、云南省重点研发项目、国家自然科学基金及云南省特色植物提取实验室开放研究基金等资助。
文章链接
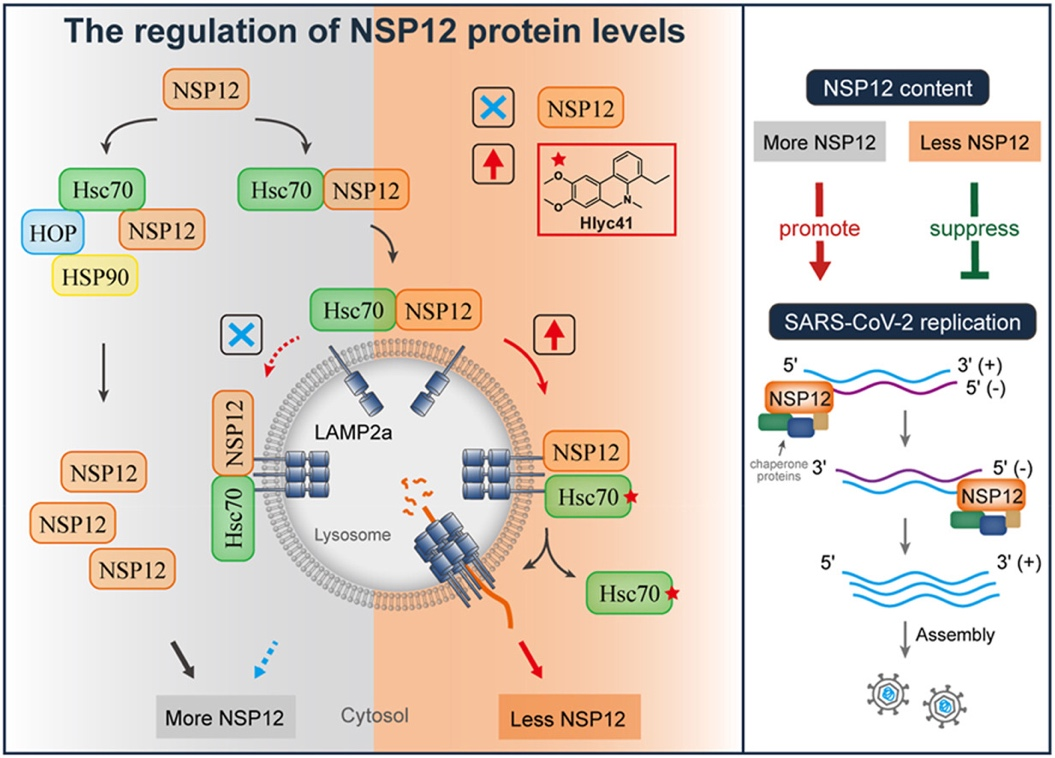
SARS-CoV-2 NSP12劫持宿主Hsc70以逃避降解并促进自身积累并进一步鉴定出Hlyc41作为靶向该劫持机制的抗病毒探针
|

